问题
填空题
将Cu投入足量的FeCl3的水溶液中,两者发生反应的化学方程式如下:
2FeCl3+Cu═2FeCl2+CuCl2
(1)请用双线桥法标出电子转移的方向和数目.
(2)在该反应中,氧化剂是______,氧化产物是______.
(3)当有0.3mol电子发生转移时,发生反应的Cu的质量为______g.
(4)请将以上反应改写为离子方程式______.
答案
(1)化合价升高元素是Cu,失电子,化合价降低元素是Fe,得到电子,化合价升高数=化合价降低数=转移电子数=2,双线桥法,电子转移的方向和数目如下:
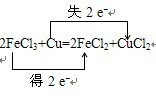
,故答案为:

;
(2)化合价降低元素Fe元素所在的反应物FeCl3是氧化剂,对应产物FeCl2是还原产物,化合价升高元素Cu所在的反应物是还原剂,对应产物CuCl2 是氧化产物,故答案为:FeCl3;CuCl2;
(3)根据方程式当有2mol电子发生转移时,发生反应的Cu的物质的量是1mol,当有0.3mol电子发生转移时,发生反应的
Cu的物质的量是0.15mol,质量是0.15mol×64g/mol=9.6g,故答案为:9.6;
(4)反应2FeCl3+Cu=2FeCl2+CuCl2改为离子方程式为:2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+.
