某化学兴趣小组利用图一装置制取氨气并探究氨气的有关性质。
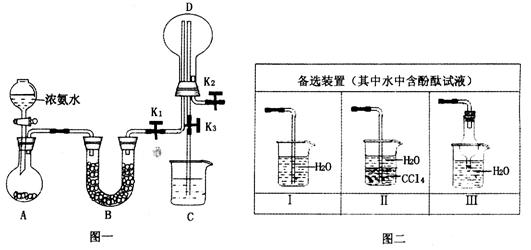
(1)装置A中烧瓶内试剂可选用________(填序号)
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱
(2)若探究氨气的溶解性,需在K2的导管末端连接图二装置中的_____装置(填序号),当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是______________
___________________________________________________________________________。
(3)若探究氨气的还原性,需打开K1、K2,K3处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成气体必须通过盛有____________试剂的洗气瓶;
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为___________________________________;
③从K3处导管逸出的气体中含有少量Cl2,则C装置中应盛放_________溶液(填化学式),反应的离子方程式为____________________________________。
(1)ace(2分,全对得2分,错选不得分)
(2)Ⅱ或Ⅲ(2分)用热毛巾将烧瓶捂热(1分)
(3)①饱和食盐水、浓硫酸(2分)
②3Cl2+8NH3=6NH4Cl+N2(2分,分布写也可)
③NaOH(1分)Cl2+2OH‾=Cl‾+ClO‾+H2O
题目分析:(1)碱石灰、生石灰、烧碱都能促进浓氨水中氨气的挥发,故ace正确。
(2)Ⅱ或Ⅲ能防止氨气的倒吸;因为装置中没有胶头滴管,所以用热毛巾捂热烧瓶,使氨气膨胀,与水接触溶解,形成喷泉。
(3)①制取的氯气中含氯化氢、水分,用饱和食盐水可除氯化氢、用浓硫酸可除水分,得到纯净、干燥的氯气。②产生的白烟为氯化铵,无色无味的气体为氮气,配平既得方程式。③氯气有毒,会污染环境,故用氢氧化钠溶液吸收尾气中的氯气,防止污染。
