问题
填空题
现有A、B、C、D、E、F六种化合物,已知它们的阳离子有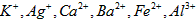 ,阴离子有
,阴离子有
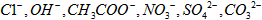 ,现将它们分别配成
,现将它们分别配成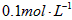 的溶液,进行如下实验:
的溶液,进行如下实验:
① 测得溶液A、C、E呈碱性,且碱性为A>E>C;
② 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③ 向D溶液中滴加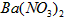 溶液,无明显现象;
溶液,无明显现象;
④ 向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
根据上述实验现象,回答下列问题
(1)实验②中反应的化学方程式是__________________
(2)E溶液是_________,判断依据是_____________________
(3)写出下列四种化合物的化学式:A_______、C_______、D_______、F_______。
答案
(1)AgNO3+NH3·H2O==AgOH+NH4NO3
(2)碳酸钾;由①中碱性强弱顺序可知E是碳酸盐,六种阳离子中与碳酸根形成可溶性盐的只有钾离子,所以E为碳酸钾
(3)Ba(OH)2;Ca(CH3COO)2;AlCl3;Fe(SO4)2
