氨水是一种的常用的化学试剂。
(1)以浓氨水和生石灰为原料,用如下装置为发生装置,可制取少 量氨气。已知:NH3·H2O+CaO=Ca(OH)2+NH3↑。
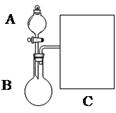
①生石灰应该装在 (填A或B)。
②试从电离平衡角度分析该实验中氨气逸出的原因: 。
③现要用试管和必要实验用品收集一试管氨气,请在C处补充相应收集装置。
(2)化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显。影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:因素一:银氨溶液的pH大小;
因素二: 。
②你设计实验验证上述影响因素一,完成下表中内容。
提供试剂:乙醛、2%稀氨水、 0.25mol/L NaOH溶液、盐酸 、 2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
| 实验步骤 | 实验操作 | 预期现象及结论(步骤1只填现象) |
| 1 | 在A、B两支洁净的试管中各入1mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水,至最初产生的沉淀恰好完全溶解,此时制得pH均约为8的银氨溶液。 | |
| 2 |
(3)吸取20.00ml 上述氨水于锥形瓶,滴加3滴甲基橙指示剂,用0.0050mol/L标准硫酸滴定,滴定至出现红色为终点,重复3次实验,平均消耗标准硫酸20.04 ml,计算上述氨水的物质的量浓度
(1) ①B
②CaO与水反应生成Ca(OH)2,溶液中OH—浓度增大,使NH3+H2O  NH4++OH—平衡逆向移动,有利于NH3逸出
NH4++OH—平衡逆向移动,有利于NH3逸出
③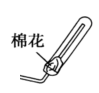
(2)①反应(水浴)的温度
②
| 实验步骤 | 实验操作 | 预期现象及结论(步骤1只填现象) |
| 1 | 先出现白色沉淀后沉淀溶解 | |
| 2 | 往A、B试管加入3滴乙醛,然后在A试管中加多1滴NaOH溶液;振荡后将两支试管放在热水浴中温热。 | 若A试管比B试管出现的银镜时间短、光亮,则溶液pH大,反应速率快;若A试管比B试管出现的银镜时间长,则溶液pH大,反应速率慢. |
(3) 0.01002 mol/L (每空2分,共16分)
题目分析:(1)①生石灰是固体应装在B圆底烧瓶里,
②氨水中存在NH3+H2O  NH4++OH—平衡,加入生石灰,可以与水反应生成Ca(OH)2,溶液中OH—浓度增大,有利于平衡逆向移动,氨气逸出;
NH4++OH—平衡,加入生石灰,可以与水反应生成Ca(OH)2,溶液中OH—浓度增大,有利于平衡逆向移动,氨气逸出;
③氨气的密度比空气小,用向下排空气法收集,同时在试管口塞一团棉花,防止与空气对流,制取的氨气不纯,装置如图
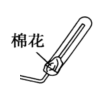
(2)①影响乙醛银镜反应速率的因素还可能有反应温度的控制;
②银氨溶液的配制过程中会看到先有白色沉淀产生,后沉淀溶解;
验证因素1,可以做对照试验,往A、B试管加入3滴乙醛,然后在A试管中加多1滴NaOH溶液;振荡后将两支试管放在热水浴中温热。比较二者出现银镜的时间,来判断溶液的pH的大小对银镜反应的影响。若A试管比B试管出现的银镜时间短、光亮,则溶液pH大,反应速率快;若A试管比B试管出现的银镜时间长,则溶液pH大,反应速率慢
(3)溶液变红,说明硫酸与一水合氨完全反应生成硫酸铵,根据2NH3·H2O~H2S04,得n(NH3·H2O)=2×20.04×10-3×0.0050mol/L,所以c(NH3·H2O)= n(NH3·H2O)/20.00×10-3L=0.01002 mol/L
