有一瓶澄清的溶液,其中可能含有NH4+、K+、 Ba2+、Al3+、Fe3+、 I-、NO3-、CO32-、
SO42-、AlO2-。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性。
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③另取溶液适量,逐滴加入NaOH溶液,现象如下:
a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀逐渐溶解,直至消失; d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
④取适量③得到的碱性溶液加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)仅由③可证明_________离子存在;写出c、d所涉及的化学反应方程式,是离子反应的用离子方程式表示:c_______________;d________________。
(2)综合判断填空:
①上述澄清溶液中一定存在的离子有_____________
②可能存在的离子有_________,检验该离子是否存在的方法为__________。
(1)Al3+、NH4+;c.Al(OH)3 +OH-=AlO2- + 2H2O;d.NH3·H2O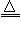 NH3↑+H2O
NH3↑+H2O
(2)①H+、NH4+、Ba2+、Al3+、I-(答不答H+都给分);②K+; 做焰色反应实验,并通过蓝色钴玻璃观察火焰的颜色,若有浅紫色,说明存在K+,若无浅紫色,说明不存在K+ 。
