问题
计算题
实验室有一种含有少量二氧化硅杂质的石灰石样品,某同学想准确测定该样品的纯度,他取用2.0 g样品于烧杯中,把20.0 mL稀盐酸分4次加入,充分作用后记录烧杯中固体质量如下表。请选择合适的数据并计算:
| 次序 | 稀盐酸/Ml | 剩余固体/g |
| 1 | 先加入5.0 mL | 1.32 |
| 2 | 再加入5.0 mL | 0.64 |
| 3 | 再加入5.0 mL | 0.20 |
| 4 | 再加入5.0 mL | 0.20 |
(2)求所取用的稀盐酸的物质的量浓度?
(3)如果该同学选用稀硝酸测定样品纯度,你认为将对结果有何影响?
答案
(1)90% (2)2.72 mol·L-1 (3)无影响
从表中数据知最后剩余的0.20 g为SiO2,故样品纯度为 ×100%=90%。
×100%=90%。
求稀盐酸的物质的量浓度,可借用1、2两组数据,二者的剩余固体质量差(1.32 g-0.64 g)即为跟5.0 mL HCl反应的CaCO3的质量。
CaCO3 + 2HCl====CaCl2+CO2↑+H2O
100 g 2 mol
(1.32-0.64) g n(HCl)
n(HCl)=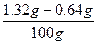 ×2 mol=1.36×10-2 mol
×2 mol=1.36×10-2 mol
c(HCl)=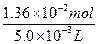 ="2.72" mol·L-1
="2.72" mol·L-1
因稀HNO3也不与SiO2反应,只跟CaCO3反应,故对结果没有影响。
