问题
实验题
如图所示是小明在学习浮力时,在课上做的几个探究性实验的主要操作情景.请问:
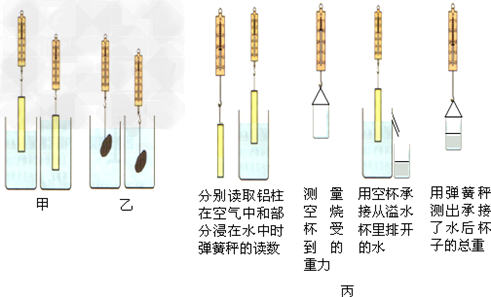
(1)图甲的两个对比性实验,是为了探究浮力的大小与 _________ 是否有关.
(2)从图乙的两个对比性实验中,你能得到的结论是 _________ .
(3)图丙是小明为了探究部分浸入液体中的物体受到的浮力大小是否符合阿基米德原理的结论而进行的几次实验,他每次操作的目的均用文字写在了操作图的下方.根据图示情况分析,小明的操作是否恰当,为什么
答案
(1)排开液体体积;
(2)物体受到的浮力与浸入液体的深度无关;
(3)不恰当;在第一步记录铝柱浸入水中弹簧测力计的拉力不合适。
