1L某混合溶液,可能含有的离子如表:
| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32-、AlO2- |
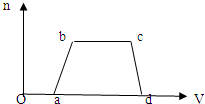
确定含有的离子是______,一定不含有的阳离子是______,一定不存在的阴离子是______,b→c的离子方程式为______.
(2)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| n(I-) | amol | 0 | 0 |
②原溶液中Cl-、Br-、I-的物质的量浓度之比为______.
(1)根据图象,开始加入NaOH没有沉淀和气体产生,则一定有H+;后来有沉淀产生且最后消失,则一定没有Mg2+、Fe2+、Fe3+,有Al3+;b→c沉淀的质量不变,应为NH4++OH-=NH3•H2O的反应,则有NH4+;现象无法知道有无K+,因为有H+,则无CO32-、AlO2-,
故答案为:H+、Al3+、NH4+;Mg2+、Fe2+、Fe3+;CO32-、AlO2-;NH4++OH-=NH3•H2O;
(2)由于还原性:I->Br-,加入氯气2.8L时溶液中I-amol,
则说明通入2.8LCl2只发生:Cl2+2I-=I2+2Cl-,
此时n(Cl2)=
=0.125mol,消耗n(I-)=2×0.125mol=0.25mol,生成n(Cl-)=2×0.125mol=0.25mol,2.8L 22.4L/mol
此时n(Br-)=1.5mol,则说明原溶液中n(Br-)=1.5mol,
根据表数据:2.8L变成5.6L,消耗2.8LCl2的物质的量为
=0.125mol,2.8L 22.4L/mol
Cl2 +2Br-=Br2+2Cl-
0.05mol 0.1mol
Cl2+2I-=I2+2Cl-
0.075mol0.15mol
则a=0.15mol,所以原溶液中:
n(I-)=0.25mol+0.15mol=0.4mol,
n(Cl-)=1.25mol-0.25mol=1mol,
n(Cl-):n(Br-):n(I-)=1:1.5:0.4=10:15:4
故答案为:①Cl2+2I-=2Cl-+I2;②10:15:4.
