二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
| 物理性质 | 色态 | 挥发性 | 熔点 | 沸点 |
| 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
| 化学性质 | 300 ℃以上完全分解 | |||
S2Cl2+Cl2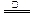 2SCl2 2SCl2 | ||||
| 遇水反应生成SO2、S等产物 | ||||

(1)仪器A的名称是 ,导管F除导气外还起的作用是 ;
(2)B中反应的离子方程式为 ;
(3)开始实验,打开分液漏斗的活塞,发现浓盐酸流出少量后即难以下滴,经检查分
液漏斗活塞没有堵塞,你认为应采取的措施是 ;
(4)装置C中的试剂是 ;如果缺少D装置,则对实验的影响是(用化学方程式表示) ;
(5)如果在加热E时温度过高,对实验结果的影响是 ;为了提高S2C12的纯度,关键的操作是控制好温度和 。
(6)设计装置H的目的是 ;烧杯中发生反应的离子方程式
是 。
(1)分液漏斗 冷凝
(2)MnO2 + 4 H+ +2 C1- ="=" Mn2+ + C12↑+ 2H2O
(3)将玻璃塞上的凹槽与漏斗口颈上的小孔对准(或拔去玻璃塞)
(4)饱和食盐水 2S2Cl2 +2H2O=SO2+3S+4HCl
(5)产率降低 控制浓盐酸的滴速不要过快
(6)吸收尾气,防止污染 C12+2OH-=Cl-+ClO-+ H2O
