水蒸气通过灼热的煤所产生的混和气,其主要成份是CO、H2还含有CO2和水蒸气.请用下列装置设计一个实验,以确认上述混和气中含有CO和H2.
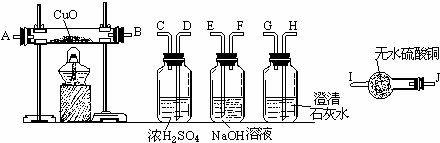
(1)连接上述装置的正确顺序是:(填各接口的代码字母)
混和气→______接______接______接______接______.
(2)确认混和气中含有H2的实验现象是______;其理由是______.
(1)由分析可知,为了验证混合气中含有CO和H2,所以实验仪器的连接先后顺序为:除二氧化碳→除掉水分→还原装置→检验水分→检验二氧化碳.①先吸收二氧化碳除掉二氧化碳的干扰;再除掉水分,排除原有水分的干扰;②还原氧化铜以后,先检验水;再检验二氧化碳;此顺序不能颠倒.
故答案为:EF→DC→AB→JI→HG;
(2)因为氢气具有还原性,能和氧化铜反应生成水,水能使无水硫酸铜变蓝,所以确认混合气中含有H2的实验现象是:黑色氧化铜变成红色铜,并且无水硫酸铜变蓝.
故答为:黑色氧化铜变成红色铜,无水硫酸铜变蓝;H2通过灼热的CuO后生成铜和水蒸气,水蒸气使无水硫酸铜变蓝.
