请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷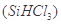 还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
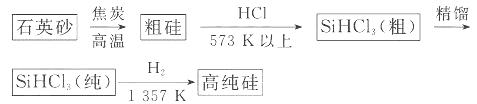
①写出由纯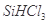 制备高纯硅的化学方程式: ____________________________________。
制备高纯硅的化学方程式: ____________________________________。
②整个制备过程必须严格控制无水无氧。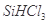 遇水剧烈反应生成
遇水剧烈反应生成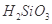 、HCl和另一种物质,配平后的化学反应方程式为___________________________;
、HCl和另一种物质,配平后的化学反应方程式为___________________________;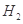 还原
还原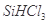 过程中若混入
过程中若混入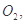 可能引起的后果是____________________________________。
可能引起的后果是____________________________________。
(2)下列有关硅材料的说法正确的是_________ (填字母)。
A.碳化硅化学性质稳定,可用于生产耐高温水泥
B.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
C.高纯度的二氧化硅可用于制造高性能通讯材料——光导纤维
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高E.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
(3)硅酸钠水溶液俗称水玻璃。取少量硅酸钠溶液于试管中,逐滴加入稀硝酸,振荡。写出实验现象并给予解释 。
(1)①
 Si+3HCl
Si+3HCl
②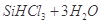

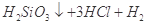 ↑ 发生爆炸
↑ 发生爆炸
(2)BC
(3)有白色胶状沉淀生成,反应原理为 Na2SiO3 + 2HNO3 = H2SiO3↓+ 2NaNO3
题目分析:(1)①根据原子守恒即质量守恒可以写出SiHCl3与H2反应的化学方程式。
②SiHCl3和H2O剧烈反应生成H2SiO3、HCl和另一种物质,分析它们化合价的变化可知,  ,而Cl的化合价未发生变化,因此另一种元素即H元素的化合价必定降低,即另一种物质是H2。
,而Cl的化合价未发生变化,因此另一种元素即H元素的化合价必定降低,即另一种物质是H2。
(2)SiC和Si3N4均为原子晶体,熔点高,性质稳定,A、B正确。光导纤维的材料为SiO2,C正确。玻璃是一种玻璃态物质,无固定的熔点。盐酸不能与硅反应,而HCl在573 K以上的温度下可与硅发生反应。因此D、E都不正确。
(3)有白色胶状沉淀生成,HNO3的酸性大于硅酸,所以发生反应:Na2SiO3 + 2HNO3 = H2SiO3↓+ 2NaNO3。
