某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
【提出猜想】
(1)猜想1:______________________________,
猜想2:______________________________,
猜想3:______________________________。
为了验证猜想,该小组设计实验加以探究:
【实验探究】该小组同学按如图所示装置,将气体从a端通入,则:
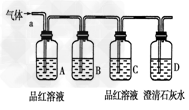
(2) B中可以装下列________试剂(填编号)。
A.NaCl溶液 B.KMnO4溶液 C.盐酸 D.澄清石灰水 E.NaHCO3 溶液 F.碘水
(3) A中品红溶液的作用是:_________________________________。
(4) D中澄清石灰水的作用是:_________________________________。
通过该实验,该小组同学观察到以下三个实验现象:
①A中品红溶液褪色 ②C中品红溶液不褪色 ③D中澄清石灰水变浑浊
【得出结论】
(5) 由上述现象该小组同学确认该气体的成分为:______________________。
(6) 请写出SO2与氯水发生反应的离子方程式:_________________________。
(1)气体为CO2;气体为SO2;气体为CO2和SO2的混合气体
(2)BF
(3)证明混合气体中是否含有SO2
(4)证明混合气体中是否含有CO2
(5)气体为CO2和SO2的混合气体
(6)Cl2+SO2+2H2O===4H++2Cl–+SO42-
