Speakers of different languages not only describe the world differently but think about it differently too, according to a new study.
Researchers used a cartoon cat Sylvester to study how language was reflected (反映) in the gestures people made. Dr. Sotaro Kita of the University of Bristol’s Department of Experimental Psychology (心理学), showed the cartoon to a group of native English, Japanese and Turkish speakers and then watched their gestures as they described the actions they had seen. He found speakers of the three different languages used different gestures to describe the same event, which appeared to reflect the way the structure of their languages expressed that event. For example, when describing a scene where the cat swings on a rope, the English speakers used gestures showing an arc trajectory (弧形轨迹) and the Japanese and Turkish speakers tended to use straight gestures showing the motion but not the arc.
Dr. Kita suggests this is because Japanese and Turkish have no proper verb to express the English meaning “to swing”. While English speakers use the arc gesture as their language can readily express the change of location and the arc-shaped trajectory, Japanese and Turkish speakers cannot as easily express the idea of movement with an arc trajectory so they use the straight gesture.
Dr. Kita said, “My research suggests that speakers of different languages cause different spatial (空间的) images of the same event in a way that matches the expressive possibilities of their own languages. In other words, language influences (影响) spatial thinking at the moment of speaking.”
68. 小题1:Researchers watched the gestures the people made because they wanted to know _____.
A.how language was reflected
B.whether they could express the same idea
C.whether they could describe what they had seen
D.how the structure of language changed69. 小题2:After watching the gestures of speakers of the three different languages, Dr. Kita concluded that _____.
A.Japanese and Turkish people couldn’t express the meaning of “swing”
B.English was obviously better than Japanese and Turkish
C.no word in Japanese and Turkish could express some ideas of English
D.every language had its own special way to describe things70.小题3:What is mainly discussed in the text?
A.Differences between languages.
B.Differences between gestures.
C.How people use different gestures to express the same event.
D.That language influences the way people think.
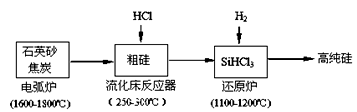
 Si + 2CO↑(2分)、SiO2 + 3C
Si + 2CO↑(2分)、SiO2 + 3C SiC + 2CO↑(2分)
SiC + 2CO↑(2分) SiHCl3 + H2(2分)
SiHCl3 + H2(2分) Si + 3HCl (2分)
Si + 3HCl (2分) Si + 2CO↑、SiO2 + 3C
Si + 2CO↑、SiO2 + 3C SiC + 2CO↑
SiC + 2CO↑ SiHCl3 + H2
SiHCl3 + H2 Si + 3HCl
Si + 3HCl
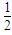 mgtgθ
mgtgθ mgsinθ
mgsinθ