I.常压下乙醇的沸点为78.5℃,乙酸的沸点为118℃,以下是分离乙醇、乙酸的方案,请填空[(1)(3)是药品,(2)(4)是操作名称]
填空:(1)______(3)______(4)______
II.下图装置是用燃烧法来确定有机物组成的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成(已知:C中的氧化铜是确保有机物中的碳元素完全转化为二氧化碳;A中的反应为2H2O2=2H2O+O2↑ ).
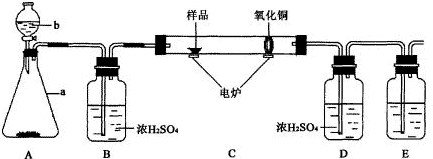
回答下列问题:
(1)A装置中a仪器的名称______,b中盛放的物质是______(填化学式).
(2)若去掉B装置会对什么元素的测量结果有影响?______(填元素符号)
(3)E装置中所盛放物质最好选用______(选填:①氢氧化钙溶液 ②氢氧化钠溶液③水)
(4)若准确称取1.12g样品(样品只含C、H、O三种元素中的两种或三种).经充分 燃烧后,D装置增重1.44g,E装置增重3.52g,则该有机物样品中所含的元素为______(填元素符号).
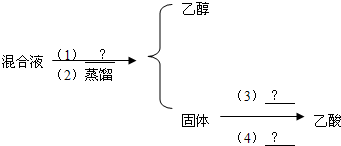
I 实验室分离乙醇和乙酸,为达到较好的分离效果,可在混合液中加入氧化钙或氢氧化钠是乙酸生成盐,进行蒸馏分离可分离乙醇和乙酸盐,乙酸为弱酸,加入硫酸后在蒸馏条件下可的乙酸.
故答案为:(1)氧化钙或氢氧化钠;(3)浓硫酸或硫酸溶液;(4)蒸馏;
II.:(1)结合课本可知该仪器为锥形瓶,根据题意:A中的反应为2H2O2
2H2O+O2↑,双氧水是液体,二氧化锰是固体,故答案为:锥形瓶;H2O2; MnO2 .
(2)分析实验设计思路可知,B装置是用来吸收A中的水蒸气,若去掉B装置,从A中挥发出来的水会进入D中,对氢元素的测量结果会有影响,故答案为:H;
(3)E装置中所盛放物质最好选用氢氧化钠溶液,因为氢氧化钠易溶于水,氢氧化钙微溶于水,氢氧化钠溶液可以完全吸收反应生成的二氧化碳,故答案为:②;
(4)D装置增重1.44g,说明反应生成了1.44g水;E装置增重3.52g,说明反应生成了3.52g二氧化碳.
1.44g水中含有的氢元素、氧元素的质量分别为:
1.44g×
×100%=0.16g,1.44g×2 18
×100%=1.28g.16 18
3.52g二氧化碳中碳元素的质量为:3.52g×
×100%=0.96g.12 44
有机物样品中碳元素和氢元素的质量和为:0.16g+0.96g=1.12g.由此说明该样品中只含有碳元素和氢元素.
故答案为:C和H.
