下列装置或操作能达到实验目的是( )
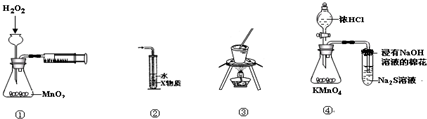
A.装置①可用于测定H2O2分解的反应速率
B.装置②中X为苯,可用于吸收氨气或氯化氢
C.装置③可用于实验室从食盐水中提取氯化钠
D.装置④可用于证明氧化性:KMnO4>Cl2>S
A.利用排水测定生成氢气的体积,测定乙醇与钠反应(放热)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目,该装置能实现实验目的,故A正确;
B.苯的密度比水小,苯应在水的上层,所以装置②中X不可能为苯,故B错误;
C.坩埚为一陶瓷深底的碗状容器,当有固体要以大火加热时,就必须使用坩埚,而本题的目的是从食盐水中提取食盐,应该用蒸发皿,故C错误;
D.高锰酸钾与浓盐酸反应,2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,化合价升高的Cl元素被氧化,对应产物Cl2是氧化产物,化合价降低的Mn元素被还原,所在的反应物KMnO4是氧化剂,所以氧化性:KMnO4>Cl2,反应Cl2+2Na2S=2NaCl+2S中,化合价升高的S元素被氧化,对应产物硫单质是氧化产物,化合价降低的Cl元素被还原,所在的反应物Cl2是氧化剂,所以氧化性:Cl2>S;所以,装置④可用于证明氧化性:KMnO4>Cl2>S,故D正确;
故选D.
