氯化铵是一种重要的化工原料,应用广泛.
(1)实验室通常用NH4Cl固体与Ca(OH)2固体混合共热制取氨气.
①写出实验室制取氨气的反应方程式______
②浓氨水可以用来检验有毒气体氯气的泄漏,反应式为3Cl2+8NH3=N2+6NH4Cl,在该反应中,氧化剂是______(填化学式),检测时观察到的现象是______,21.3g氯气能氧化氨气______mol.
(2)用浓氯化铵溶液处理的舞台幕布难着火,其原因是______(填字母).
①幕布的着火点升高
②幕布的质量增加
③氯化铵分解吸收热量,降低了温度
④氯化铵分解产生的气体隔离了部分空气
A.①②B.③④C.①③D.②④
(3)实验室可用NH4Cl溶液与饱和的NaNO2溶液反应制取纯净的氮气,反应方程式为:NaNO2+NH4Cl
NaCl+N2↑+2H2O △ .
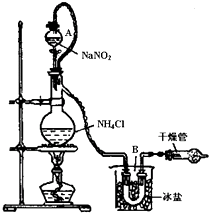
实验装置如图所示,试回答:
①装置中A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是______(填写编号).
a.防止饱和溶液蒸发
b.保证实验装置不漏气
c.使饱和NaNO2溶液容易滴下
②加热前必须进行的一个操作步骤是______.
③收集N2最适宜的方法是______(填写编号)
a.排空气法收集在集气瓶中
b.排水法收集在集气瓶中
c.直接收集在球胆或塑料袋中.
(1)①实验室用氯化铵和氢氧化钙固体加热来制氨气,原理方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2 △ .
CaCl2+2NH3↑+2H2O; △ .
②反应3Cl2+8NH3=N2+6NH4Cl中,化合价降低的元素是Cl,所在的反应物Cl2是氧化剂,氯气和氨气相遇因生成大量的氯化铵固体颗粒而产生白烟,氯气和被氧化的氨气的量的关系是:3Cl2~2NH3,21.3g氯气即0.3mol氯气能氧化氨气0.2mol,故答案为:Cl2;有大量白烟产生;0.2;
(2)氯化铵溶液容易水解,然后生成的氯化氢和氨气易挥发,吸热,同时生成的氯化氢和氨气隔离了部分空气,
故答案为:B;
(3)①装置中A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起到了平衡气压的作用,可以让饱和NaNO2溶液容易滴下,故选c;
②装置加热前,一定要检查气密性,故答案为:检查气密性;
③氮气的密度和空气相近,不能用排空气法,难溶于水,可以用排水法,结合实验的简单程度,直接收集在球胆或塑料袋中更简便易行,故答案为:c.
