问题
问答题
某小组设计实验,探究NO2被水吸收,力求达到:①NO2尽可能全部吸收 ②集气瓶中残留的气体尽可能少.
(1)实验室常用Cu和浓HNO3反应来制取,其化学方程式为______
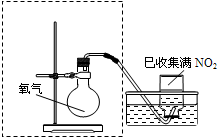
(2)如图虚线框内是某同学设计的装置简图,请你补充画出其中缺少的一种仪器(含试剂)______.
(3)根据设计的实验完成下表.
| 实验步骤 | 实验现象 | 化学方程式 | |
| ① | 将收集满NO2的集气瓶倒立 在水槽中 | ||
| ② | 气体由无色变成红棕色, 后又变成无色,液面继 续上升 | ||
| ③ | 其它现象与上相同.最后 瓶内只含极少量气体,液 体几乎充满 |
答案
(1)Cu与浓硝酸反应生成硝酸铜、二氧化氮和水,该反应为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
(2)该反应为固体与液体的反应,需要分液漏斗加液体,分液漏斗中盛有浓硝酸,如图

,故答案为:

;
(3)二氧化氮溶于水,发生3NO2+H2O=2HNO3+NO,观察到集气瓶中液面上升约三分之二,气体由红红棕色变成无色,进行操作②通入氧气发生2NO+O2=2NO2,重复操作②,总反应为4NO2+O2+2H2O=4HNO3,则液体几乎充满集气瓶,
故答案为:
| ① | 集气瓶中液面上升约三分 之二,气体由红红棕色变 成无色 | 3NO2+H2O=2HNO3+NO 2NO+O2=2NO2 | |
| ② | 将水逐滴滴入烧瓶,向盛有 NO2的集气瓶通入少量氧气 后,停止通气 | ||
| ③ | 多次重复第②步操作,依次 减少氧气通入量,直至氧气 通入后,气体不变成红棕色 |




