氮及其化合物在工农业生产中具有重要作用.
(1)某小组进行工业合成氨N2(g)+3H2(g)⇌2NH3(g)△H<0的模拟研究,在1L密闭容器中,分别加入0.1molN2和0.3molH2.实验①、②、③中c(N2)随时间(t)的变化如图所示.
实验②从开始到达到平衡状态的过程中,用H2表示的平均反应速率为______.
与实验①相比.实验②所采用的实验条件可能为______(填字母),实验③所采用的实验条件可能为______(填字母).
a.增大压强b.减小压强c.升高温度d.降低温度e.使用催化剂
(2)NH3可用于处理废气中的氮氧化物,其反应原理为2NH3(g)+NO(g)+NO2(g)⇌2N2(g)+3H2O(g)△H<O,
欲提高废气中氮氧化物的转化率,可采取的措施是______(填字母)
a.升高温度b.增大压强c.增大NH3的浓度
(3)NCl3遇水发生水解反应,生成NH3的同时得到______(填化学式).ClO2是广谱高效消毒剂,制备原理为NCl3+6ClO2-+3H2O=NH3↑+6ClO2+3OH-+3Cl-.若转移1mol电子,则制取ClO2的质量为______.
(4)25℃时,将amol•L-1的氨水与bmol•L-1盐酸等体积混合,反应后溶液恰好显中性,则a______b(填“>”、“<”或“=”).用a、b表示NH3•H2O的电离平衡常数为______.
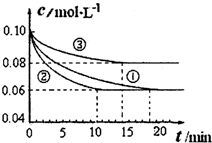
(1)由图可知,实验②10min到达平衡,平衡时△(N2)=0.1mol/L-0.06mol/L=0.04mol/L,由方程式可知,△c(H2)=3△(N2)=3×0.04mol/L=0.12mol/L,故v(H2)=
=0.012mol/(L•min),0.12mol/L 10min
由图可知,与实验①相比,实验②到达平衡所以时间较短,反应速率较快,但平衡时氮气的浓度不变,改变条件平衡不移动,该反应正反应是气体体积减小的反应,增大压强平衡会移动,故实验②应是使用催化剂,
由图可知,与实验①相比,实验③到达平衡所以时间较短,反应速率较快,平衡时氮气的浓度增大,改变条件平衡逆向移动,该反应正反应是体积减小的放热反应,故为升高温度;
故答案为:0.012mol/(L•min),e,c;
(2)提高废气中氮氧化物的转化率,应改变条件使平衡向正反应移动,
a.该反应正反应是放热反应,升高温度,平衡向逆反应移动,氮氧化物的转化率降低,故a错误;
b.该反应正反应是体积增大的反应,增大压强,平衡向逆反应移动,氮氧化物的转化率降低,故b错误;
c.增大NH3的浓度,平衡向正反应移动,氮氧化物的转化率增大,故c正确;
故答案为:c;
(3)NCl3遇水发生水解反应,NCl3分子中负价原子结合水电离的氢离子,正价原子结合水电离的去氢根离子,故生成NH3的同时还得到HClO,
反应中只有氯元素的化合价发生变化,氯元素由NCl3中+1降低为Cl-中-1价,由ClO2-中+3价升高为ClO2中+4价,故转移1mol电子,生成ClO2的物质的量为1mol,质量为1mol×67.5g/mol=67.5g,
故答案为:HClO,67.5;
(4)溶液显中性,所以c(H+)=c(OH-),溶液的电荷守恒可得:c(H+)+c(NH4+)=c(Cl-)+c(OH-),故c(NH4+)=c(Cl-),氯化铵是强酸弱碱盐其水溶液呈酸性,要使氯化铵溶液呈中性,则氨水应稍微过量,因为盐酸和氨水的体积相等,则氨水的物质的量浓度大于盐酸,
溶液中c(H+)=c(OH-)=10-7mol/L,c(NH4+)=c(Cl-)=
mol/L,c(NH3•H2O)=(b 2
-a 2
)mol/L,b 2
电离常数只与温度有关,则此时NH3•H2O的电离常数Kb=
=c(N
)•c(OH-)H +4 c(NH3•H2O)
=
×10-7b 2
-a 2 b 2
,b×10-7 a-b
故答案为:>,
.b×10-7 a-b
