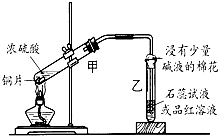
浓硫酸与铜的反应用了如图所示的装置,请回答下列问题.
(1)若试管乙中装的是石蕊试液,则反应过程中观察到乙中的现象是______;若试管乙中装的是品红溶液,则反应过程中观察到乙中的现象是______.
(2)反应结束后在试管甲的底部常可见到一些白色固体,该固体可能是______ (填化学式).待试管甲内液体冷却后,将试管中的液体慢慢倒入另一支盛有少量水的试管中,观察溶液的颜色.这一步操作的目的是要证实______.
(3)写出上述试管甲中发生反应的化学方程式______,若收集到标准状况下气体0.56L,则反应中转移电子的物质的量为______.
在加热条件下铜与浓硫酸发生:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O, △ .
(1)二氧化硫为酸性气体,与水反应生成H2SO3,溶液呈酸性,可使石蕊试液变红,具有漂白性,可使品红褪色,
故答案为:石蕊试液变红;品红溶液褪色;
(2)反应生成CuSO4,为白色固体,溶于水溶液呈蓝色,为Cu2+的颜色,故答案为:CuSO4;溶液中有Cu2+存在;
(3)反应的化学方程式为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,n(SO2)= △ .
=0.025mol,0.56L 22.4L/mol
则转移的电子的物质的量为2×0.025mol=0.05mol,
故答案为:0.05mol.
