硫酸是一种实验室常用的化学试剂.请按要求填空:
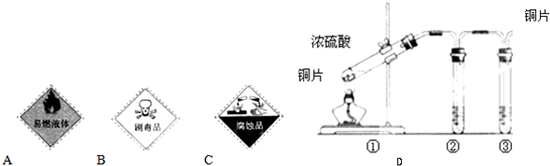
(1)浓硫酸试剂瓶上适合贴上的图标是______(填写字母标号).
(2)实验室有1.00mol•L-1的硫酸溶液,从中准确量出10.00mL,其物质的量浓度为______mol•L-1.现将准确量出的10.00mL的硫酸溶液配制成0.100mol•L-1的稀硫酸,所需要的玻璃仪器除烧杯、玻璃棒还需______和______.
(3)用图D所示的实验装置验证铜与浓硫酸反应生成的气体产物,则装置②、③试剂依次为下列的______和______
A.品红溶液B.BaCl2溶液 C.NaOH溶液D.AgNO3溶液
(4)装置①中发生反应的化学方程式为______,若装置①中加入铜6.4g和含有0.2molH2SO4的浓硫酸,则产生二氧化硫质量______
A.等于6.4克B.大于6.4克C.小于6.4克D.不能确定
(5)若将装置①中的铜片换成木炭,装置②试管内为品红溶液,装置③试管内为澄清石灰水,则装置①中发生反应的化学方程式为______.装置②中的现象是______.根据装置③观察到有白色沉淀生成的现象,______(填“能”或“不能”)判断该白色沉淀一定只有CaCO3.
(1)浓硫酸具有腐蚀性,适合贴上的图标是图中的C,故答案为:C;
(2)溶液为稳定、均一的分散系,则实验室有1.00mol•L-1的硫酸溶液,从中准确量出10.00mL,其物质的量浓度应仍为1.00mol•L-1,将准确量出的10.00mL的硫酸溶液配制成0.100mol•L-1的稀硫酸,应将体积稀释为100mL,则配制溶液时用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管以及100mL容量瓶等仪器,
故答案为:1.00;胶头滴管;100mL容量瓶;
(3)铜和浓硫酸反应生成二氧化硫,二氧化硫具有漂白性,可先后品红检验,因二氧化硫有毒,不能排放到空气中,可用氢氧化钠吸收,故答案为:A;C;
(4)铜和浓硫酸在加热条件下发生氧化还原反应,反应的方程式为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,随着反应的进行,硫酸浓度逐渐降低,稀硫酸和铜不反应,则生成的二氧化硫小于0.1mol,质量小于6.4g,△ .
故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;C;△ .
(5)碳和浓硫酸在加热条件下发生氧化还原反应生成二氧化碳和二氧化硫,反应的方程式为C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,生成的二氧化硫可使品红溶液由红色变为无色,因二氧化硫和二氧化碳都能与氢氧化钙溶液反应生成沉淀,则不能断该白色沉淀一定只有CaCO3.△ .
故答案为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;溶液由红色变为无色;不能.△ .
