问题
计算题
某校研究性学习小组得到一块铁制品,不知它是生铁还是钢,几位同学设计了一个实验来进行鉴定。他们用200ml稀盐酸(密度为1.04g/cm3)分四次加入到金属块上,生成的氢气能被完全收集起来进行称量,实验数据记录在下表(此块制品假设只是由铁和单质碳两种物质组成的,碳不与盐酸反应也不溶于盐酸)。生铁含碳质量分数为2%~4.3%。

仔细阅读分析表中数据后解答:
(1)第 次加入盐酸并充分反应后, 制品中的铁和盐酸恰好完全反应。
(2)通过计算回答:这块铁制品中单质碳的质量分数为多少?它是生铁还是钢?
(3)求所用的盐酸溶液中HCl的质量分数?
答案
(1) 3
(2)解:设制品中Fe的质量为x,三次参加反应的HCl质量为y
依据题意得:
Fe + 2HCl=== FeCl2 + H2↑
56 73 2
x y 0.6
所以

解之得:x=16.8g y=21.9g
C%=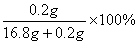 ≈1.18% 是钢
≈1.18% 是钢
(3)HCl%=
