取m1g某常见粉末(由M、Z两种元素组成)进行如下实验。将该粉末和足量碳粉充分混合,平铺在反应管a中,b瓶中盛足量澄清石灰水。按图连接仪器并检查好气密性。
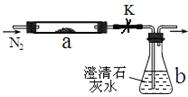
实验开始时,先进行操作G,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。经一系列测定,确定反应完全后,停止加热,继续通氮气,直到反应管冷却。此时,管中的熔融物凝固成银白色金属M,再进行分离、提纯、称量,得到m2g纯金属M,且m1=1.38m2。根据以上叙述回答问题:
(1)该粉末的化学式是_________ ____;操作G是______________________。
____;操作G是______________________。
(2)停止加热前是否需要先关闭止水夹K?_________;原因:_____________。
(3)反应管a中产生金属单质的化学方程式为:__________________________。
 (4)本实验的尾气是否需处理?_______;如需处理,请回答如何处理;如不需处理,
(4)本实验的尾气是否需处理?_______;如需处理,请回答如何处理;如不需处理,
请说明理由。_______________________________________________。
(5)在题目“一系列测定”中,当连续_____________时,则可确定反应管中反应已完全。
(6)某同学做该实验时,b瓶最终得到了澄清溶液,他向该溶液中加入了某物质,溶液又出现了浑浊。请书写出现浑浊的离子方程式:___________________________。
(11分)
(1)Fe3O4;缓缓通入氮气(2分)
(2)不需要。因为停止加热后仍继续通N2,不会发生倒吸。(2分)
(3) Fe3O4+4C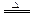 3Fe+4CO↑,或F
3Fe+4CO↑,或F e3O4+2C
e3O4+2C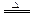 3Fe+2CO2↑,
3Fe+2CO2↑,
或Fe3O4+4CO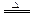 3Fe+4CO2↑ (1分)
3Fe+4CO2↑ (1分)
(4)需要处理,因为生成了有毒的CO。 (1分)
可连接一个加热的装有CuO粉末的反应管(或放一个点燃的酒精灯,或用一气球收集气体。其它合理答案同样给分)。(1 分)
分)
(5)两次称量反应管及反应混合物总质量的差值不超过0.001g。(2分)
(6)Ca2++HCO3—+OH—→CaCO3↓+H2O(2分)(其他合理答案也给分)如加Ba(OH)2
