问题
计算题
某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成。分四次取样品与稀硫酸反应,其实验数据记录如下表。
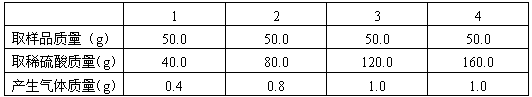
试计算:
⑴第 次反应是锌和硫酸恰好完全反应。
⑵黄铜中锌的质量分数。
答案
(1)3
(2)设Zn的质量为x
Zn+H2SO4===ZnSO4+H2↑
65 2
x 1g
65/2=x/1g x= 32.5g
黄铜屑中锌的质量分数:32.5g/50g×100%=65%
答:黄铜屑中锌的质量分数为65%
某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成。分四次取样品与稀硫酸反应,其实验数据记录如下表。

试计算:
⑴第 次反应是锌和硫酸恰好完全反应。
⑵黄铜中锌的质量分数。
(1)3
(2)设Zn的质量为x
Zn+H2SO4===ZnSO4+H2↑
65 2
x 1g
65/2=x/1g x= 32.5g
黄铜屑中锌的质量分数:32.5g/50g×100%=65%
答:黄铜屑中锌的质量分数为65%