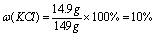草木灰是农村常用的一种钾肥,其中只有其有效成分K2CO3能溶于水。实验中学化学兴趣小组的同学为了测定某草木灰中K2CO3的含量,称取该草木灰100g用足量的水将其溶解。经过滤. 洗涤(洗液并入滤液中)后,将滤液蒸发至80.4g时停止加热并冷至室温,再向其中逐滴加入稀盐酸,同时将生成的CO2用足量的石灰乳[Ca(OH)2]吸收。加入盐酸的质量m与石灰乳中增加的质量△m的关系如图所示。
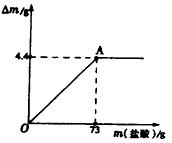
(1)写出坐标中曲线上A点的含义:______________________________________________ __________________________________________________________;
(2)草木灰中K2CO3的质量分数和所用稀盐酸中溶质的质量分数各是多少?
(3)滤液中的K2CO3与盐酸恰好完全反应时所得的溶液中,溶质的质量分数是多少?
解:(1)①滤液中的K2CO3恰好和盐酸中的HCl此时恰好完全反应(定性)
②73g盐酸与滤液中的K2CO3恰好完全反应时,生成CO2的质量为4.4g(定量)
(2)设滤液中含K2CO3的质量为x,73g盐酸中含HCl的质量为y,生成的KCl的质量为z
K2CO3 + 2HCl===2KCl + CO2↑+ H2O
138 73 149 44
x y z 4.4g
138:44=x:4.4g 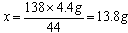
73:44=y:4.4g 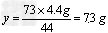
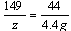
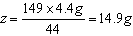
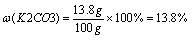

(3)恰好完全反应时溶液的质量为:80.4g+73g-4.4g=149g