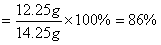问题
计算题
将氯酸钾与二氧化锰的混合物14.25g装入大试管中,加热制取氧气。充分反应后,大试管中的固体残留物的质量为9.45g。计算:
(1)反应生成的氧气的体积为多少升(此时32g氧气的体积为22.4L)?
(2)大试管中的固体残留物里,二氧化锰的质量为多少克?
(3)原14.25g混合物中,氯酸钾的质量分数为多少(精确到1%)?
答案
解:生成O2的质量=14.25g-9.45g= 4.8g
生成O2的体积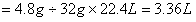
设反应中生成氯化钾的质量为x
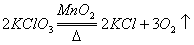
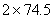
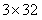
x 4.8g
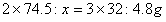
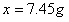
 的质量
的质量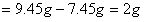
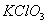 的质量
的质量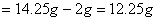
 的质量分数
的质量分数