问题
计算题
蒸馒头用的某纯碱中含有少量的氯化钠,为了测定该纯碱中碳酸钠和氯化钠的含量,取一定量的该纯碱样品全部溶解在100g水中,再加入氯化钙141g,恰好完全反应。(反应方程式为Na2CO3+CaCl2===
CaCO3+2NaCl)经过滤、干燥后称得沉淀质量为10g,所得滤液中氯化钠的质量分数为5%,请计算:
①纯碱样品中碳酸钠的质量;
②纯碱样品中氯化钠的质量。
答案
解:设样品中碳酸钠的质量为x,样品中氯化钠的质量为y,反应生成氯化钠的质量为z。
Na2CO3+CaCl2===CaCO3↓+2NaCl
106 100 117
x 10g z
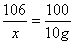 解得x=10.6g
解得x=10.6g
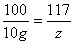 解得z=11.7g
解得z=11.7g
![]() ×100%=5%
×100%=5%
解得y=0.4g
答:纯碱样品中碳酸钠的质量为10.6g,氯化钠的质量为0.4g。
