问题
计算题
钙是维持人体正常功能所必需的元素。右图所示为某种补钙剂“钙尔奇”说明书的一部分。取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应)。烧杯内物质质量变为11.34g。试计算:
(1)每片钙尔奇中含碳酸钙的质量。
(2)服用这种补钙剂,每人每天摄入钙元素的质量。
(3)所用稀盐酸中溶质的质量分数。

答案
解:(1)设每片钙尔奇中含碳酸钙的质量为x,
根据反应前后质量守恒,可知生成CO2的质量为10g+2.0g-11.34g=0.66g
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 44
X 0.66g
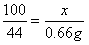
解得 x=1.5g
(2)由(1)可知,每片钙尔奇中碳酸钙的质量为1.5g,其中钙元素质量为
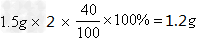
(3)设所用稀盐酸中溶质的质量分数为y
CaCO3+2HCl===CaCl2+H2O+CO2↑
73 44
10g×y 0.66g
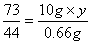
解得y=10.95%
