问题
计算题
某研究性学习小组在探究Na2CO3和K2CO3性质时发现它们的性质相似,如何鉴别它们呢?通过查询资料,得知它们都能跟稀硫酸反应,反应的化学方程式如下:
Na2CO3 + H2SO4 == Na2SO4 + H2O + CO2↑和K2CO3 + H2SO4 == K2SO4 + H2O + CO2↑
小组同学取Na2CO3和K2CO3 各10.6g,分别进行如下实验:
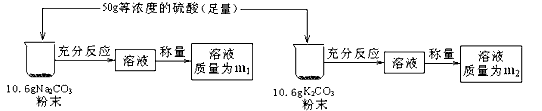
请通过计算得出:(若不能整除,结果精确到0.1)
(1)10.6gNa2CO3完全反应生成CO2质量与10.6gK2CO3完全反应生成CO2的质量哪个多?
(2)反应后所得溶液的质量m1和m2哪个大?经测定,实验值与理论值相符合。通过上述实验他们知道了可用此法鉴别Na2CO3和K2CO3。
答案
(1)10.6g Na2CO3完全反应生成CO2质量为4.4g
10.6g K2CO3完全反应生成CO2的质量为3.4g
所以10.6g Na2CO3完全反应生成的CO2质量多。
(2)m1=56.2g
m2=57.2g
所以m2>m1
