问题
计算题
Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
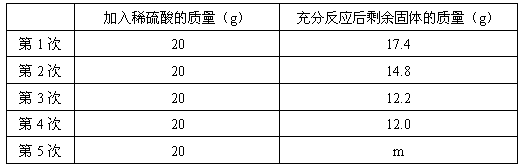
试回答下列问题:
(1)上述表格中m的值为 ;
(2)黄铜样品中锌的质量分数为 ;
(3)所用稀硫酸中硫酸的质量分数是多少?
答案
(1)12.0(或12)
(2)40%
解:设所用稀硫酸中硫酸的质量分数为x
Zn + H2SO4 === ZnSO4 + H2↑
65 98
20g-17.4g=2.6g 20gx
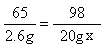 x=19.6%
x=19.6%
答:所用稀硫酸中溶质的质量分数为19.6%。
