问题
计算题
为了测定某铜锌合金中锌的质量分数,某同学利用该合金与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下:
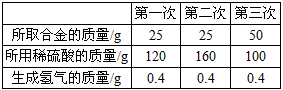
(1)试计算该铜锌合金中锌的质量分数。
(2)从上表数据分析,当所取合金与所用的稀硫酸的质量比为 时,表示合金中的锌与稀硫酸中的硫酸恰好完全反应。请简述理由。
答案
(1)52%
(2)1:4
理由:由(1)中的分析可知:25克合金与足量的稀H2SO4反应放出H2 0.4g,而第三次实验中50g合金与100g稀H2SO4混合反应后也放出H2 0.4g,说明50g合金中只有25g参加了反应,表明此时稀H2SO4已经反应完全,即25g合金中的锌能与100g稀H2SO4恰好完全反应,质量比=25g:100g=1:4
