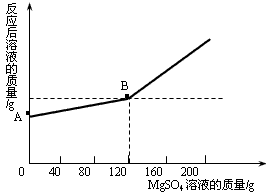
已知金属钠和水能发生下列反应:2Na+2H2O=2NaOH+H2↑ 现取金属钠4.6 g投入到100 g水中,充分反应后,冷却到室温(20℃),得到一种不饱和溶液,向所得溶液中逐滴滴入MgSO4溶液,实验测得溶液的总质量与滴入MgSO4溶液的质量关系曲线如图所示。根据题意回答下列问题:
⑴金属钠和水充分反应后,生成氢气的质量为 g。
⑵图中A点的纵坐标表示的溶液的质量是 g。
⑶通过计算求出当滴入120gMgSO4溶液时,所得溶液中溶质的质量分数是多少?(计算结果精确至0.1%)
⑴ 0.2
⑵ 104.4
解:设生成NaOH的质量为x。
2Na+2H2O===2NaOH + H2↑
46 80
4.6g x
46∶80 = 4.6g∶x x = 8g
设 最终生成Na2SO4的质量为y,生成 Mg(OH)2的质量为z。
MgSO4+2NaOH===Na2SO4+Mg(OH)2↓
80 142 58
8g y z
80∶142 = 8g∶y y = 14.2g
80∶58 = 8 g∶z z = 5.8g
反应后溶液的总质量为:4.6g+100g+120g-5.8g-0.2g=218.6g

答:反应后的溶液中溶质的质量分数为6.5%
