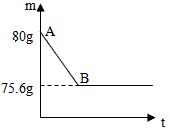
某兴趣小组为了测定鸡蛋壳(主要成分是碳酸钙)中CaCO3的含量,取14g鸡蛋壳,捣碎,放在烧杯中,再加入66g的稀盐酸,恰好完全反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中反应的剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水分的蒸发)。
求:(1)产生CO2的质量为多少?(2)该鸡蛋壳中CaCO3的质量?(3)所得溶液的溶质质量分数?
解: (1)产生CO2的质量:80g-75.6g=4.4g
(2)设鸡蛋壳中含CaCO3的质量为X;反应生成CaCl2的质量为Y。
CaCO3+2HCl = CaCl2+H2O+CO2↑
100 111 44
X Y 4.4g
100/X=44/4.4g X=10g
111/Y=44/4.4g Y=11.1g
(3)反应后所得溶液的质量:10g+66g-4.4g=71.6g
所得溶液的溶质质量分数:11.1g/71.6g×100%=15.5%
答:产生CO2的质量为4.4g;该鸡蛋壳中CaCO3的质量为10g;所得溶液的溶质质量分数15.5%。
