近年来,江苏省酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(1)有人提出了一种利用氯碱工业产品治理含二氧化硫废气的方法,流程如下:
(I)将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液。
(II)将电解饱和食盐水所得气体反应后制得盐酸。
(III)将盐酸加入NaHSO3溶液中得SO2气体回收,生成的NaCl循环利用。
① 写出步骤(I)反应的化学方程式:_______________
② 写出步骤(III)反应的离子方程式:___________________
(2)还有学者提出利用 Fe2+、Fe3+等离子的催化作用,常温下将SO2氧化成SO42-而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO42-的转化率。
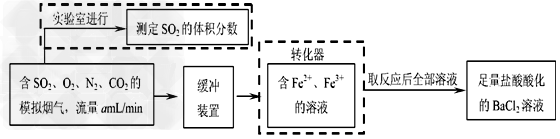
① 该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是(填序号)_______________。(参考:还原性SO2 > I- >Br->Cl-)
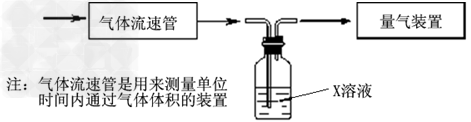
A.碘的淀粉溶液
B.酸性高锰酸钾溶液
C.氢氧化钠溶液
D.氯化钡溶液
② 若上述实验是在标准状况下进行的,X是已知体积和物质的量浓度的溶液,欲测定转化器中SO2氧化成SO42-的转化率,已知气体流速,还需测定的数据是__________和加入盐酸酸化的氯化钡溶液后生成沉淀的质量。
(3) 为进一步减少SO2的污染并变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2。该方法涉及到的化学反应为:SO2+2CO=2CO2+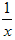 Sx、CO+
Sx、CO+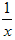 Sx=COS、2COS+SO2=2CO2+
Sx=COS、2COS+SO2=2CO2+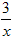 Sx。其中COS中“C”化合价为__________。
Sx。其中COS中“C”化合价为__________。
(4)若生活污水中含大量的氮化合物,通常用生物膜脱氮工艺进行处理:首先在消化细菌的作用下将NH4+氧化为NO3-:NH4++2O2=NO3-+2H++H2O,然后加入甲醇(CH3OH),NO3-和甲醇转化为两种无毒气体。请写出加入甲醇后反应的离子方程式__________________________。
(1)SO2+NaOH=NaHSO3;HSO3-+H+==SO2↑+H2O
(2)AB;实验时间
(3)+4
(4)5CH3OH+6NO3-+6H+ ==5CO2↑+3N2↑+13H2O
