问题
计算题
对煤燃烧后的烟气进行脱硫处理的主要反应原理为:2SO2+2CaCO3+4H2O+O2==2CO2+2CaSO4·2H2O(石膏)。某处理厂现有125t含杂质的石灰石,若运用上述原理吸收SO2气体,测量数据如下表:
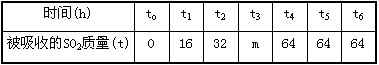
试计算:
(1)表中m为____,
(2)完全反应后被吸收的SO2质量为____,
(3)计算该石灰石中碳酸钙的质量分数。
答案
(1)48
(2)64t
(3)设该石灰石中碳酸钙的质量为x。
2SO2+2CaCO3+4H2O+O2==2CO2+2CaSO4·2H2O
128 200
64t x
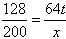 ;x=100t
;x=100t

答:该石灰石中碳酸钙的质量分数为80%。
