问题
计算题
小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用的办法如下:取用8g这种石灰石样品,把40g稀盐酸分4次加入,测量过程所得数据见下表(已知石灰石样品中含的杂质不溶于水,不与盐酸反应)。
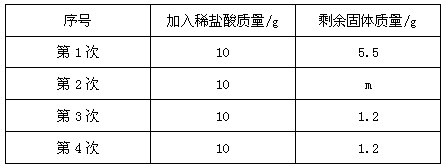
请计算:
(1)8g石灰石样品中含有杂质多少克?
(2)样品中碳酸钙的质量分数是多少?
(3)下表中m的数值应该为多少?
(4)要得到280kgCaO,需要质量分数为80%的石灰石多少千克?(化学方程式:CaCO3 CaO+CO2↑)
CaO+CO2↑)
答案
(1)8g石灰石样品中含有杂质为1.2g。
(2)样品中碳酸钙的质量分数=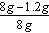 =85%。
=85%。
(3)m=5.5g-(8g-5.5g)=3g
(4)设需要80%的石灰石的质量为x。
CaCO3 CaO+CO2↑
CaO+CO2↑
100 56
x×80% 280kg
 ;x=625kg
;x=625kg
