问题
计算题
取了13.3g氢氧化钠固体样品加适量的水配成溶液,向其中加入200g10%的稀盐酸,使其充分反应,生成二氧化碳2.2g。
求:
⑴样品中氢氧化钠的质量;
⑵和氢氧化钠反应的盐酸的质量;
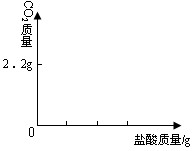
⑶在下图中画出以纵坐标表示二氧化碳质量,横坐标表示盐酸的质量的关系图。(已知Na2CO3+2HCl==2NaCl+H2O+CO2↑)
答案
(1)解:设固体样品中碳酸钠的质量为x,跟碳酸钠反应的盐酸的质量为y。
Na2CO3+2HCl==2NaCl+H2O+CO2↑
106 73 44
x y×10% 2.2g
106:x=73:(y×10%)=44:2.2g
x=5.3g;y=36.5g
NaOH的质量为:13.3g-5.3g=8g
(2)设和氢氧化钠反应的盐酸的质量为z。
NaOH+HCl==NaCl+H2O
40 36.5
8g z×10%
40:36.5=8g:(z×10%)
z=73g
(3)
