问题
计算题
一定质量的20%的烧碱溶液和一定质量的硫酸镁溶液恰好完全反应,所得溶液的质量为109.2g,其中溶质的质量分数为13%,计算硫酸镁溶液中溶质的质量分数。(计算过程保留两位小数)
答案
硫酸钠的质量为109.2g×13%=14.2g
解:设反应的硫酸镁的质量为x,氢氧化钠的质量为y,生成的氢氧化镁质量为z。
2NaOH+MgSO4==Mg(OH)2↓+Na2SO4
80 120 58 142
x y z 14.2g
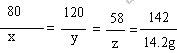
x=8g;y=12g;z=5.8g
烧碱溶液的质量为8g÷20%=40g
硫酸镁溶液的质量为109.2g+5.8g -40g=75g
硫酸镁溶液的溶质质量分数为12g÷75g×100%=16%
