问题
填空题
工业上用电解饱和食盐水的方法制取氢氧化钠、氯气和氢气,但电解前要进行粗盐精制。试回答下列问题:
资料卡片:
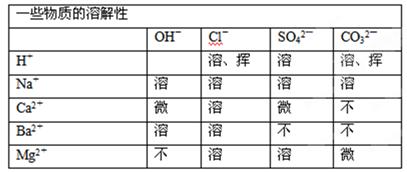
(1)选择试剂以除去下表所列的可溶性杂质。
| 杂质 | 加入的试剂 |
| CaCl2 | Ⅰ________ |
| MgCl2 | Ⅱ________ |
| 硫酸盐 | Ⅲ________ |
(3)最后加适量的盐酸以调节溶液至中性并除去过量的CO32—.其中盐酸除去CO32—的化学方程式为______________________________________________________________________.
答案
(1)Ⅰ.Na2CO3 Ⅱ.NaOH Ⅲ.BaCl2 (2)Ⅲ、Ⅰ
(3)Na2CO3+2HCl=2NaCl+CO2↑+H2O
(1)由于不能再引入新的杂质,所以可用碳酸钠用来除去Ca2+;氢氧化钠用来除去Mg2+;氯化钡用来除去SO42-。
(2)由于过量的氯化钡需要通过碳酸钠来除去,因此碳酸钠必须放在氯化钡的后面,即正确顺序是Ⅲ、Ⅰ。
(3)盐酸的酸性强于碳酸的,所以盐酸和碳酸钠反应的方程式为
Na2CO3+2HCl=2NaCl+CO2↑+H2O。

 Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化
Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化