问题
计算题
现有一包只含有氯化钙杂质的粗盐样品。某校化学兴趣小组的同学为测定该粗盐样品中氯化钙的质量分数,称取该粗盐样品10g,充分溶解于100mL水中(水的密度是1g/cm3),再滴加适量的碳酸钠溶液,产生沉淀的质量与加入碳酸钠溶液的质量关系如下图所示。试计算:
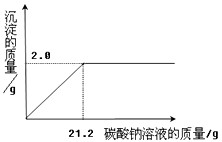
(1)该粗盐样品中氯化钙的质量分数。
(2)过滤后所得滤液中溶质的质量分数。(精确到0.1%)
答案
解:设粗盐样品中氯化钙的质量为x,生成的NaCl质量为y。
则Na2CO3+CaCl2==CaCO3↓+2NaCl
111 100 117
x 2.0g y
x=2.22g,y=2.34g
(1)粗盐样品中氯化钙的质量分数=2.22g/10g×100%=22.2%
(2)滤液的溶质质量分数= ×100%=7.8%
×100%=7.8%
