我市充分发挥自己的区域优势,积极打造“海西铜都”。某铜业从国外进口一批含碱式碳酸铜[Cu2(OH)2CO3]70%以上的孔雀石作原料,为检测碱式碳酸铜含量是否达到要求,技术人员取孔雀石样品30g与溶质质量分数为20%的稀硫酸反应,反应过程中产生CO2和消耗稀硫酸的情况如下图所示。

[温馨提示]①反应原理是Cu2(OH)2CO3+2H2SO4==2CuSO4+3H2O+CO2↑;②孔雀石中其他 物质不与稀硫酸反应;③Cu2(OH)2CO3的相对分子质量为222。
请解答下列问题:
(1)实验室常用98%的浓硫酸稀释得到稀硫酸,稀释时应先将_____(填“浓硫酸”或“水”)倒入容器中。
(2)该样品中含碱式碳酸铜的质量是多少?
(3)通过计算,判断样品中含碱式碳酸铜的质量分数是否达到要求?
(1)水
(2)解:样品中含碱式碳酸铜的质量为x。
方法一:Cu2(OH)2CO3+2H2SO4==2CuSO4+3H2O+CO2↑
222 44
x 4.4g
222:44=x:4.4g
解得x=22.2g
答:样品中含碱式碳酸铜的质量为22.2g。
方法二:Cu2(OH)2CO3+2H2SO4==2CuSO4+3H2O+CO2↑
222 196
x 98g×20%
222:196=x:(98g×20%)
解得x=22.2g
答:样品中含碱式碳酸铜的质量为22.2g。
(3)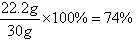
74%大于70%
答:样品中碱式碳酸铜的含量达到要求。
