问题
计算题
某化工厂生产的纯碱产品中含有少量氯化钠杂质,为测定该产品中含碳酸钠的质量分数,某课外兴趣小组进行了以下实验。取一定质量的该纯碱样品于试管中,加入85.6g稀盐 酸,恰好完全反应,产生8.8g气体。经测定,所得溶液常温下为不饱和溶液,溶液中含钠元素的质量为10.0g。请你据此分析计算:
(1)该产品中碳酸钠的质量分数是____。
(2)反应后所得溶液中溶质的质量分数。
答案
(1)91. 4%
(2)解:设碳酸钠的质量为x,生成氯化钠的质量为y。
Na2CO3+2HCl==2NaCl+H2O+CO2↑
106 117 44
x y 8.8g
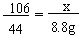 ,x=21.2g
,x=21.2g
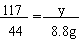 ,y=23.4g
,y=23.4g
设所得溶液中溶质的质量为m。
Na--NaCl
23 58.5
10.0g m
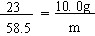
m=25.4g
58.5m原样品中NaCl的质量为:25.4g -23.4g=2.0g
所得溶液的质量为:21.2g+2.0g+85.6g-8.8g=l00.0g
所得溶液中溶质的质量分数为:25.4g/100.0g×100%=25.4%
