问题
计算题
某同学用过氧化氢溶液和二氧化锰制取氧气,化学方程式为:2H2O2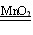 2H2O+O2↑,该同学将50g过氧化氢溶液和1g二氧化锰混合,完全反应后,称量剩余的混合物质量为49.4g。求:
2H2O+O2↑,该同学将50g过氧化氢溶液和1g二氧化锰混合,完全反应后,称量剩余的混合物质量为49.4g。求:
(1)反应产生氧气的质量是______g。
(2)该同学所用过氧化氢溶液的溶质质量分数是多少(列式计算)?
答案
解:(1)反应产生氧气的质量=(50g+1g)-49.4g=1.6g
(2)设50g过氧化氢溶液中含H2O2的质量为X
2H2O2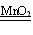 2H2O+O2↑
2H2O+O2↑
68 32
X 1.6g
因为:32X=68×1.6g
所以:X=3.4g
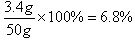
答:过氧化氢溶液的溶质质量分数为6.8%。
(合理即可)
