问题
计算题
黄铜是铜和锌的合金。为了测定某黄铜样品中铜的质量分数,取20g该黄铜样品加入一定量稀硫酸中(Zn+H2SO4==ZnSO4+H2↑),恰好完全反应,产生氢气0.2g。求:
(1)该黄铜样品中锌的质量。
(2)该黄铜样品中铜的质量分数(精确到0.1﹪)。
答案
(1)解:设样品中锌的质量为X
Zn+H2SO4==ZnSO4+H2↑
65 2
X 0.2g
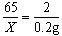 ;X=6.5g
;X=6.5g
(2)铜的质量分数=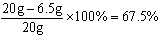
答: 样品中锌的质量为6.5g;铜的质量分数是67.5%。
