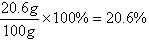问题
计算题
现有含CaCl2和NaCl两种物质的固体混合物20g,加水完全溶解得到混合溶液60g,再向该溶液中加入Na2CO3溶液50g,这时恰好完全反应,过滤,得到100g滤液(假设过过程中溶液质量无损失)。试计算:
(1)求原固体混合物中CaCl2的质量;
(2)滤液中溶质的质量分数。
答案
解:碳酸钙的质量=60g+50g-100g=10g
设混合物中CaCl2的质量为x,生成的NaCl的质量为y。
CaCl2+Na2CO3==2NaCl+CaCO3↓
111 117 100
x y 10g

x=11.1g
y=11.7g
溶液中溶质的质量为:11.7g+(20g-11.1g)=20.6g
溶液中溶质的质量分数为: