问题
计算题
向202克硫酸铜溶液中加入一定量铁粉恰好完全反应,经过滤、烘干,得到干燥的固体物质16克。试求:原加入的铁粉质量是多少?最后得到溶液的溶质质量分数是多少?
答案
解:设原加入的铁粉质量是x,生成的硫酸亚铁质量为y
Fe+CuSO4==FeSO4+Cu
56 152 64
x y 16g
56﹕64=x﹕16g
x=14g
152﹕64=y﹕16g
y=38g
最后得到溶液中溶质硫酸亚铁的质量分数为: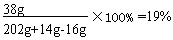
答:原加入的铁粉质量是14g,生成的硫酸亚铁质量为19%。
