问题
计算题
某校化学兴趣小组为测定某硝酸铵样品的纯度,将10g样品溶于30g水后,再加入13.7g氢氧化钠浓溶液共热,两者恰好完全反应(硝酸铵中的杂质不与氢氧化钠反应,也不溶于水,硝酸铵与氢氧化钠的反应方程式为:NH4NO3+NaOH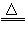 NaNO3+H2O+NH3↑)。把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质量,结果如下表所示:
NaNO3+H2O+NH3↑)。把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质量,结果如下表所示:
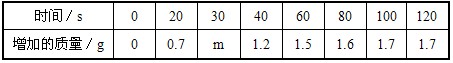
试回答下列问题:
(1)请在下面的坐标纸上,以反应时间为横坐标,以产生的NH3质量为纵坐标,画出能够表明产生气体的质量随时间变化的关系曲线;
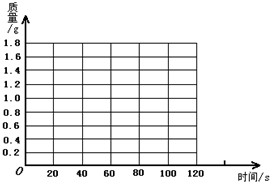
(2)表中m约为______;
(3)硝酸铵样品的纯度为__________;
(4)试计算反应后所得硝酸钠溶液的溶质质量分数(不考虑反应过程中水损失的质量)。
答案
(1)曲线图要求:曲线平滑、趋势正确、给出平台
(2)1.0g
(3)80%
(4)解:设纯净硝酸铵的质量为x
NH4NO3+NaOH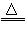 NaNO3+H2O+NH3↑
NaNO3+H2O+NH3↑
85 17
x 1.7g
85/17=y/1.7g
y=8.5g
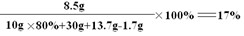
答:反应后所得溶液的溶质质量分数为17%。
