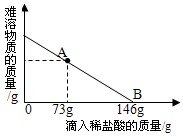
在一烧杯中盛有42.2gCaCO3和CaCl2的粉末状混合物,向其中188.8g水,使混合物中的可溶物完全溶解。然后再向其中逐滴加如溶质的质量分数为10%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如图所示。
请根据题意回答下列问题:
(1)在滴入稀盐酸的过程中,观察到的明显现象是:
①________________________ ,②_________________________。
(2)当滴入10%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是(写化学式)___________。
(3)当滴入10%的稀盐酸146g时(即B点),试通过计算,求此时烧杯中所得不饱和溶液的质量。(计算结果精确到0.1g)
(1)①固体物质不断溶解;②有气体产生(或有气泡冒出)
(2)CaCl2
(3)解:146g10%的稀盐酸中含有HCl的质量是:146g×10%=14.6g
设反应中生成CO2的质量为x。
CaCO3+2HCl==CaCl2+H2O+CO2↑
73 44
14.6g x
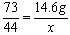 ;x=8.8g
;x=8.8g
烧杯里所得不饱和溶液的质量为:188.8g+42.2g+146g-8.8g=368.2g
答:烧杯里所得不饱和溶液的质量为368.2g。(其他合理方法可给分)
