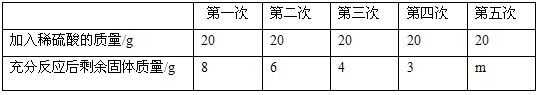
现有氧化铜和铜的混合物,对其成分进行分析。取10g此样品,向其中分五次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:(反应的化学方程式:CuO+H2SO4==CuSO4+H2O)
试回答下列问题:
(1)上述表格中m的值为________,10g样品中CuO的质量为________g。
(2)计算所加入稀硫酸中溶质的质量分数?
(3)计算第三次加稀硫酸反应后所得溶液中溶质的质量分数?(精确到0.1%)
(1)3;7
(2)解:设第一次反应需H2SO4的质量为x,第三次反应后生成CuSO4的质量为y
CuO+H2SO4==CuSO4+H2O
80 98 160
(10-8)g x
(10-4)g y
80/98=2g/x
x=2.45g
80/160=6g/y
y=12g
H2SO4溶液中溶质质量分数=2.45g/20g×100%=12.25%
(3)第三次加稀硫酸反应后所得溶液中溶质质量分数=12g/(60g+6g)×100% =18.2%
答:所加入稀硫酸中溶质质量分数为12.25%;第三次加稀硫酸反应后所得溶液中溶质质量分数为18.2%。
