问题
计算题
为了测定石灰石中碳酸钙的含量,将粉碎后的15g石灰石样品(样品中杂质不溶于水,且不与酸反应)放入烧杯中,然后加入足量的盐酸完全反应。烧杯中剩余固体质量与加入盐酸质量的关系如图所示。

请计算:
(1)该石灰石样品中碳酸钙的质量分数(计算结果保留一位小数)。
(2)如果盐酸的质量分数为7.3%,求恰好反应时盐酸的质量。
答案
解:(1)分析图象可以得出:石灰石样品中不与稀盐酸反应的固体的质量有5g。
则该石灰石样品中碳酸钙的质量分数为: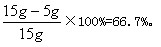
(2)设与10g碳酸钙恰好完全反应时消耗盐酸的质量为x。
CaCO3+2HCl==CaCl2+H2O+CO2↑
100 73
10g x×7.3%
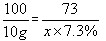
解得:x=100g
答:(1)石灰石样品中碳酸钙的质量分数为66.7%;
(2)恰好完全反应时消耗盐酸的质量为100g。
