问题
计算题
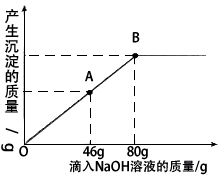
在一烧杯中盛有一定质量的MgCO3固体,向其中滴加溶质的质精分数为10%的H2SO4溶液,至恰好完全反应。得到102g不饱和溶液。向所得溶液中逐滴滴入溶质质量分数为10%的NaOH溶液,产生沉淀的质量与所滴入NaOH溶液的质量关系曲线如图所示。请根据题意回答下列问题:
(1)在滴入稀硫酸时,观察到的明显实验现象是______________________________。
(2)当滴入NaOH溶液至图中A点时,烧杯中溶液里含有的溶质是(写化学式) __________。
(3)当滴入10%的NaOH溶液80g时(即B点),试通过计算,求此时所得不饱和溶液的质量。(计算结果精确至0.1g)
答案
(1)固体物质不断溶解;有气体产生(或有气泡冒出)
(2)Na2SO4、MgSO4
(3)解:80g10%的NaOH溶液中含NaOH的质量是:80g×10%=8g
设反应中生成Mg(OH)2的质量为x
MgSO4+2NaOH==Mg(OH)2+Na2SO4
80 58
8g x
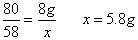
烧杯里所得不饱和溶液的质量为:102g+80g-5.8g=176.2g
答:所得溶液的质量为176.2g。(其他合理答案可得分)
